Cinètica de Michaelis-Menten
La cinètica de Michaelis-Menten descriu la velocitat de reacció de moltes reaccions enzimàtiques. El seu nom és en honor de Leonor Michaelis i Maud Menten. Aquest model només és vàlid quan la concentració del substrat és major que la concentració de l'enzim, i per a condicions d'estat estacionari, o sigui que la concentració del complex enzim-substrat és constant.
Determinació de constants
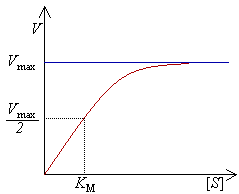
Per determinar la velocitat màxima d'una reacció enzimàtica, la concentració de substrat ([S]) és augmentada fins a aconseguir una velocitat constant de formació de producte. Aquesta és la velocitat màxima (VPlantilla:Petit) de l'enzim. En aquest cas, els llocs actius de l'enzim estan saturats amb substrat.
Velocitat de reacció/velocitat V
La velocitat V indica el nombre de reaccions per segon que són catalitzades per un enzim. Amb concentracions creixents de substrat[S], l'enzim va acostant-se asimptòticament a la seva velocitat màxima Plantilla:Color, però mai hi acaba d'arribar. Per aquesta raó, no hi ha un [S] determinat per a la Plantilla:Color. De totes maneres, el paràmetre característic de l'enzim està definit per la concentració de substrat a la qual s'arriba a la meitat de la velocitat màxima (Vmàx/2).
Constant de Michaelis 'KPlantilla:Petit'
Llavors, encara que la concentració de susbtrat a VPlantilla:Petit no pot ser medida exactament, els enzims poden ser caracteritzats per la concentració de substrat a la qual la velocitat de reacció és la meitat de la velocitat màxima. Aquesta concentració de substrat es coneix com a constant de Michaelis-Menten (KPlantilla:Petit).
Aquesta constant representa (per a enzims que exhibeixen una cinètica de Michaelis-Menten simple), la constant de dissociació (l'afinitat del complex enzim-substrat (ES) pel substrat). Valors baixos indiquen que el complex ES està unit molt fortament i rarament es dissocia sense que el substrat reaccioni per donar producte.
Així, per aquests casos, s'obtindrà una KPlantilla:Petit diferent, segons el substrat específic, en què actui cada enzim (com passa en el cas d'enzims que actuen en substrats anàlegs); i les condicions de reacció en què es realitzin les mesures.
Nota: KPlantilla:Petit només pot ésser utilitzada per a determinar l'afinitat d'un enzim per un substrat kPlantilla:Petit és limitant de la velocitat, per exemple, kPlantilla:Petit << kPlantilla:Petit i KPlantilla:Petit esdevé kPlantilla:Petit/kPlantilla:Petit. Generalment, kPlantilla:Petit >> kPlantilla:Petit, o kPlantilla:Petit i kPlantilla:Petit són comparables.
Equació
La derivació de Michaelis-Menten va ser descrita per Briggs i Haldane. S'obté de la següent manera:
Se suposa que la reacció enzimàtica és irreversible, i que el producte no es lliga amb l'enzim després de la reacció.
Seguint l'aproximació de l'estat estacionari, que assenyala que la concentració del complex enzim-substrat (ES) és petita i es manté quasi constant al llarg de la reacció enzimàtica:
Es defineix:
Llavors:
(1)
La velocitat de la reacció és:
(2)
La concentració total de l'enzim:
Conseqüentment:
(3)
Substituint (3) en (1) dona:
Reordenant:
(4)
Substituint (4) en (2) i multiplicant numerador i denominador per :
Aquesta equació pot ser analitzada experimentalment amb una representació de Lineweaver-Burk o un diagrama d'Eadie-Hofstee.
- EPlantilla:Petit és el total d'enzim. No es pràctic mesurar la quantitat de complex enzim-substrat durant la reacció, fet pel qual s'ha d'escriure en termes de quantitat total o inicial d'enzim, que és una quantitat coneguda.
- d[P]/dt o VPlantilla:Petit és la velocitat de producció de producte.
- kPlantilla:Petit[EPlantilla:Petit] o VPlantilla:Petit és la velocitat màxima. kPlantilla:Petit sovint és anomenada kPlantilla:Petit.
S'ha de tenir en compte que [S] és gran comparada amb KPlantilla:Petit, [S]/(KPlantilla:Petit + [S]) tendeix a 1. La velocitat de formació de producte és igual a kPlantilla:Petit[EPlantilla:Petit] en aquest cas.
Quan [S] és igual a KPlantilla:Petit, [S]/(KPlantilla:Petit + [S]) val 0.5. En aquest cas, la velocitat de formació de producte és la meitat de la màxima(1/2 VPlantilla:Petit). Graficant VPlantilla:Petit contra [S], es pot determinar fàcilment VPlantilla:Petit i KPlantilla:Petit. Això requereix una sèrie d'experiments a EPlantilla:Petit constant i diferents concentracions de substrat [S].